Štandardný postup pre skríning chorôb pečene na Slovensku – Spoločné odporúčania Slovenskej hepatologickej spoločnosti (SHS) a Slovenskej spoločnosti všeobecného praktického lekárstva (SSVPL)
Tomáš Koller1, Mária Szántová1, Peter Makara2
+ Pracoviště
Souhrn
Slovensko patrí na popredné miesta vo svete v prevalencii aj úmrtnosti na pokročilé choroby pečene. Keďže prirodzený priebeh ich najčastejších príčin je dlhodobý a asymptomatický, existuje veľké časové okno na identifikáciu ich rizika a zavedenie účinných preventívnych opatrení. Tento materiál má za cieľ navrhnúť lekárom v klinickej praxi základné princípy v iniciálnom skríningu chorôb pečene u asymptomatických jedincov. Odporúča v prvom rade aktívne pátranie po rizikových faktoroch najčastejších chorôb pečene, ako sú metabolický syndróm, miera konzumácie alkoholu, rizikové faktory chronických vírusových hepatitíd a stanovenie aktivity ALT v sére. Pri identifikácii rizikových faktorov ďalej odporúča diagnostické upresnenie prítomnosti steatózy pečene, vírusových hepatitíd, potvrdenie pretrvávajúcej elevácie ALT a stratifikáciu rizika fibrózy pečene. Nakoniec, tento štandardný postup navrhuje základné línie v manažmente identifikovaných rizikových faktorov a v prípade zistených chorôb pečene definuje pravidlá pre odosielanie na špecializované hepatologické vyšetrenie.
Klíčová slova
skríning, chronické choroby pečene, prevencia, rizikové faktory, štandardný postup
Tento štandardný postup bol schválený na riadnych zasadnutiach výbormi Slovenskej hepatologickej spoločnosti a výborom Slovenskej spoločnosti všeobecného praktického lekárstva.

Úvod
Chronické choroby pečene sú častou príčinou predčasných úmrtí. Ich univerzálne asymptomatický priebeh vedie k tomu, že sa až v 80 % prípadov diagnostikujú v neskorých štádiách dekompenzácie cirhózy, kedy sú efektívny manažment a prognóza už výrazne obmedzené [1]. Skorá diagnostika chorôb pečene je preto dôležitou podmienkou na zlepšenie prognózy a zníženie počtu odvrátiteľných úmrtí [2]. Vyhľadávanie chorôb je základným poslaním každého lekára, avšak skríning chorôb je najmä doménou všeobecného lekárstva. Tento štandardný postup navrhuje základné princípy skríningu chorôb pečene u ľudí bez zjavných znakov choroby pečene.
Epidemiológia
Slovensko patrí medzi krajiny s vysokou prevalenciou odvrátiteľných úmrtí. Podľa správy z roku 2022 bola mortalita na preventabilné príčiny na úrovni 193 prípadov na 100 000 obyvateľov a patrili sme medzi päť najhorších krajín OECD [2]. Choroby tráviacej sústavy s výnimkou zhubných nádorov tvorili u ľudí do 50 a 65 rokov v rokoch 2011 až 2020 približne 10 % všetkých úmrtí [3]. Podľa údajov NCZI v Zdravotníckej ročenke patrili chronické choroby pečene do troch najčastejších príčin smrti u ľudí od 25 do 65 rokov [4]. Krajiny strednej Európy vrátane Slovenska patria do regiónu so stabilne vysokou prevalenciou cirhózy. Nedávna správa o globálnom bremene chorôb pečene dokonca uvádza, že Slovensko je krajinou s najvyššou prevalenciou cirhózy na svete [5]. Údaje z nášho skríningového projektu SIRIUS ukazujú, že rizikovú konzumáciu alkoholu má 15 %, nárazové pitie aspoň raz mesačne 22 %, steatózu pečene približne 47 %, a metabolický rizikový faktor až 70 % dospelej populácie. Zvýšenie ALT nad 1,5-násobok normy malo približne 11 % populácie, prevalencia HBV infekcie sa odhaduje na 0,5–1 % u ľudí narodených pred rokom 1994 a HCV na 0,2–0,6 % populácie.
Etiológia a patogenéza
Chronické choroby pečene sú v našich podmienkach najčastejšie spôsobené škodlivou konzumáciou alkoholu, obezitou a metabolickým syndrómom, chronickou infekciou vírusmi hepatitídy B alebo C, alebo autoimunitnými chorobami pečene [6]. Patogeneticky tieto faktory poškodzujú pečeň buď cestou nadmerného ukladania tuku, teda vznikom steatózy pečene. Steatóza je najčastejším prvotným mechanizmom poškodenia pečene alkoholom a metabolickým syndrómom. Menej často pri nich dochádza aj k poškodeniu hepatocytov, teda ku vzniku zápalového poškodenia a nekrózy. Apoptóza alebo nekróza sú zvyčajne mechanizmami poškodenia pečene pri chronických vírusových hepatitídach a pri autoimunitnom poškodení. Výsledkom oboch týchto procesov je prestavba štruktúry pečene s ukladaním väziva, teda so vznikom fibrózy pečene. Spomenuté procesy ako steatóza, nekróza a fibróza môžu prebiehať aj súčasne, ale každý z nich je spočiatku do veľkej miery reverzibilný. Ak však dôjde ku nadmernej prestavbe parenchýmu pečene, dôsledkom je portálna hypertenzia. Táto môže následne viesť ku komplikáciám, ako sú dekompenzácia cirhózy (napr. ako ascites, krvácanie, encefalopatia), zlyhanie pečene, alebo hepatocelulárny karcinóm.
Prirodzený vývoj
Riziko progresie do pokročilej fibrózy, cirhózy alebo nádoru pečene je najvyššie pri kombinácii viacerých etiologických faktorov [7]. Progresia chorôb pečene je takmer vždy asymptomatická, dlhodobá a jej priebeh je nepravidelný. Alkoholová cirhóza sa najčastejšie objavuje v 4. až 6. dekáde života [8]. Menej agresívnou chorobou je steatotická choroba pečene s priemerným vekom dosiahnutia dekompenzácie cirhózy v 6. a 7. dekáde života [9]. V našom registri RH7 je až 90 % pacientov s cirhózou vo veku 30–70 rokov. Existuje preto veľké časové okno, počas ktorého je možné choroby pečene odhaliť. Odstránenie rizikových faktorov poškodzujúcich pečeň (alkohol, tuk) alebo liečba príčiny choroby pečene (antivírusová liečba, imunosupresíva), dokážu proces progresie choroby zastaviť, aj úplne zvrátiť [10].
Nástroje na skríning chorôb pečene:
1. Chronické vírusové hepatitídy je možné vyhľadávať u pacientov s rizikovými faktormi, ktoré sú uvedené v tab. 1. U jedincov s minimálne jedným rizikovým faktorom je potrebné vyšetriť krv na prítomnosť HBs antigénu a protilátok anti-HCV.

2. Steatózu pečene je možné zistiť pomocou fatty liver indexu (FLI) alebo abdominálnej ultrasonografie. Na výpočet FLI sú potrebné tieto údaje: hmotnosť, obvod pása, triacylglyceroly a hodnota GGT v sére. Hodnoty nad 60 svedčia pre steatózu pečene. Každý pacient so steatózou pečene by mal mať zároveň stanovený aj index FIB-4. Na jeho výpočet je potrebný vek, počet trombocytov, AST a ALT v sére. Oba indexy je možné zistiť použitím hepkalkulačky (hepkalkulacka.sk).
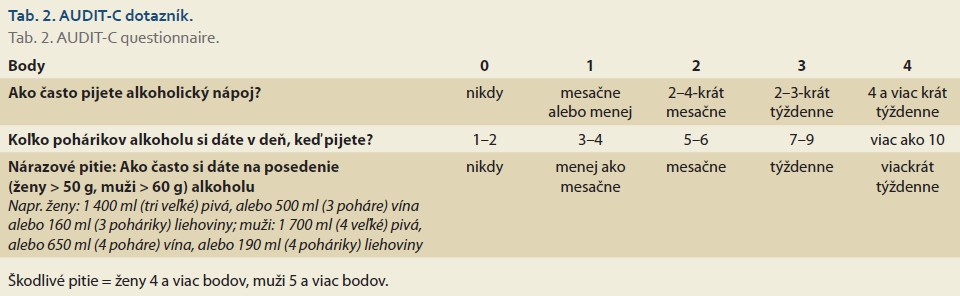
3. Na detekciu škodlivej konzumácie alkoholu slúži dotazník AUDIT-C uve- dený v tab. 2 alebo množstvo konzumovaného čistého alkoholu v gramoch za deň. Za škodlivú konzumáciu sa považuje AUDIT-C skóre ≥ 4 alebo > 20 g u žien, a ≥ 5 alebo > 30 g u mužov [11]. Napr. 20 g alkoholu obsahuje 500 ml 12° piva, 200 ml vína, 60 ml 40% destilátu. Za škodlivé pitie považujeme aj nárazové pitie, teda konzumáciu 50 g u žien alebo 60 g alkoholu u mužov na jedno posedenie 1× týždenne a častejšie (tab. 2).
4. Na správnu interpretáciu aktivity ALT je potrebné dodržať odberové podmienky uvedené v tab. 3.

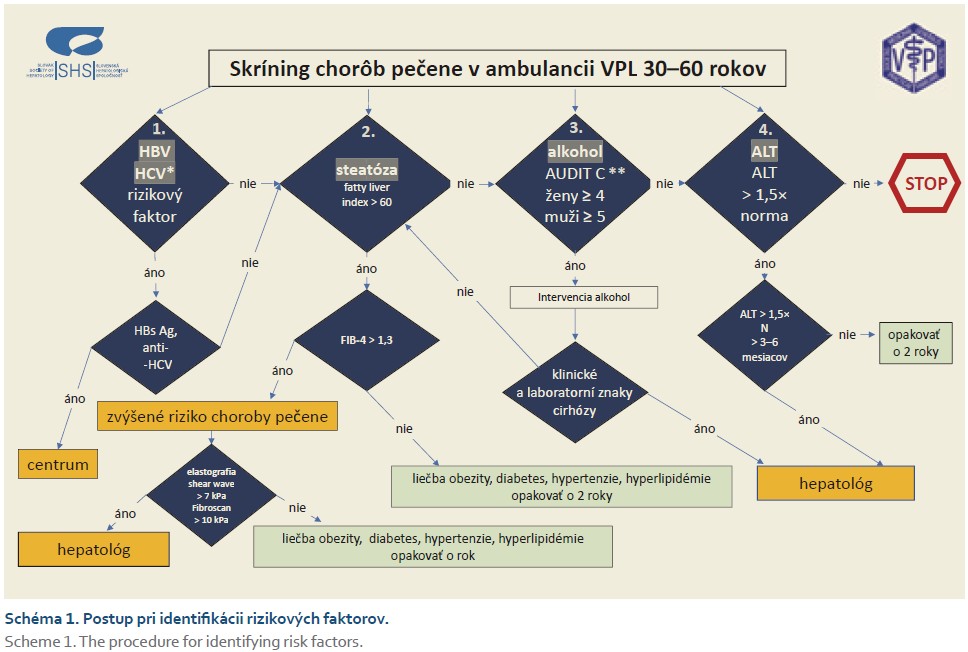
Postup pri identifikácii rizikových faktorov (schéma 1)
1. V prípade reaktívneho výsledku HBs antigénu alebo anti-HCV je potrebné pacienta odoslať do centra pre liečbu vírusových hepatitíd, ktorými sú vybrané hepatologické a infektologické pracoviská, (https://www.slovhep.sk/pracoviska/zobrazit-ambulancie).
2. V prípade zistenia steatózy pečene (FLI > 60):
a) a FIB-4 ≤ 1,3 je hlavnou preventívnou intervenciou liečba metabolických rizikových faktorov, teda obezity, hypertenzie, diabetu a hyperlipidémie;
b) a FIB-4 > 1,3 je okrem liečby metabolických rizikových faktorov vhodné pacienta odoslať na elastografické vyšetrenie pečene;
c) ak výsledok elastografie svedčí pre pokročilú fibrózu (Fibroscan > 10 kPa, alebo Shear wave elastografia > 7 kPa), pacienta je potrebné odoslať na špecializované hepatologické vyšetrenie.
3. V prípade zistenia škodlivej konzumácie alkoholu je potrebná intervencia s informáciou o multiorgánovej toxicite alkoholu. Následne je postup závislý od prítomnosti steatózy pečene. V prípade klinického podozrenia alebo objektívnych údajov závislosti od alkoholu, je potrebný komplexný multiodborový prístup.
4. V prípade zistenia elevácie ALT nad 1,5-násobok normy je potrebné test opakovať s odstupom 1–2 mesiacov. Príčinu elevácie ALT trvajúcu viac ako 3–6 mesiacov je potrebné objasniť na špecializovanej hepatologickej ambulancii.
Špeciálne situácie
Anamnéza rodinného výskytu dedičných chorôb pečene ako m. Wilson, deficit alfa 1 antitrypsínu, porfýria, alebo hemochromatóza je indikáciou na hepatologické vyšetrenie. Naopak, samotná benígna hyperbilirubinémia (m. Gilbert) nie je dôvodom na ďalšie vyšetrovanie alebo sledovanie.
Doručeno/Submitted: 17. 3. 2025
Přijato/ Accepted: 19. 3. 2025
Korešpondenčný autor
doc. MUDr. Tomáš Koller, PhD.
V. interná klinika
LF UK a UN Bratislava
Ružinovská 6
826 06 Bratislava
koller.tomas@gmail.com
Pro přístup k článku se, prosím, registrujte.
Výhody pro předplatitele
Výhody pro přihlášené
Literatura
1. Koller T, Kindlová J, Šturdík I et al. Prognostické indexy cirhózy a ich vzťah k prirodzenému priebehu a k príčinám úmrtia pacientov s cirhózou v slovenskej populácii pred érou transplantácie pečene. Trend Hepatol 2013; 5(1): 26.
2. OECD. Avoidable mortality: OECD/Eurostat lists of preventable and treatable causes of death (January 2022 version). 2022 [online]. Dostupné z: http: //www.oecd.org/health/health-systems/Avoidable-mortality-2019-Joint-OECD-Eurostat-List-preventable-treatable-causes-of-death.pdf.
3. Koller T, Baráková A. Trends in premature mortality from digestive system cancers in Slovakia in the years 2011–2020: 8 diagnoses over 10 years. Gastroent Hepatol 2023; 77(5): 394–408. doi: 10.48095/ccgh2023394.
4. NCZI. Zdravotnícka ročenka Slovenskej republiky 2020. 2020 [online]. Dostupné z: chrome-extension: //efaidnbmnnnibpcajpcglclefindmkaj/https: //www.nczisk.sk/Documents/rocenky/2020/Zdravotnicka_rocenka_Slovenskej_republiky_2020.pdf.
5. Sepanlou SG, Safiri S, Bisignano C et al. The global, regional, and national burden of cirrhosis by cause in 195 countries and territories, 1990–2017: a systematic analysis for the Global Burden of Disease Study 2017. Lancet Gastroenterol Hepatol 2020; 5(3): 245–266. doi: 10.1016/S2468-1253(19)30349-8.
6. Pimpin L, Cortez-Pinto H, Negro F et al. Burden of liver disease in Europe: epidemiology and analysis of risk factors to identify prevention policies. J Hepatol 2018; 69(3): 718–735. doi: 10.1016/j.jhep.2018.05.011.
7. Koller T, Rac M. Neinvazívne, semiinvazívne a invazívne diagnostické modality v diagnostike portálnej hypertenzie na Slovensku. Gastroenterol Prax 2015; 14(1): 18–22.
8. Planas R, Balleste B, Alvarez MA et al. Natural history of decompensated hepatitis C virus-related cirrhosis. A study of 200 patients. J Hepatol 2004; 40(5): 823–830. doi: 10.1016/ j.jhep.2004.01.005.
9. Powell EE, Cooksley WG, Hanson R et al. The natural history of nonalcoholic steatohepatitis: a follow-up study of forty-two patients for up to 21 years. Hepatology 1990; 11(1): 74–80. doi: 10.1002/hep.1840110114.
10. Marcellin P, Gane E, Buti M et al. Regression of cirrhosis during treatment with tenofovir disoproxil fumarate for chronic hepatitis B: a 5-year open-label follow-up study. Lancet 2013; 381(9865): 468–475. doi: 10.1016/S0140-6736(12)61425-1.
11. Szantova M, Koller T. S alkoholom asociovaná choroba pečene: skríning v gastroenterológii a diagnostika v kontexte s novou nomenklatúrou stukovatenia pečene. Gastroenterol Prax 2023; 22(4): 242–248.