Polymorfické formy rifaximinu a klinická účinnost
Milan Lukáš1
+ Pracoviště
Rifaximin je strukturální analog rifampicinu (4-deoxy-4-methylpyrido[1,2-1,2] imidazo[5,4-c]rifamycin), jehož antibakteriální efekt je zprostředkován blokádou syntézy bakteriální RNA, inhibicí betapodjednotky DNA dependentní RNA polymerázy. Jedná se o širokospektrálně účinné baktericidní antibiotikum blokující růst grampozitivních i gramnegativních aerobních i anaerobních bakterií. Efekt rifaximinu je cílen pouze na gastrointestinální trakt, protože léčivo vykazuje minimální reabsorpci z trávicího traktu a po podání vysokých dávek léčiva (2 × 1 g denně) dosahuje naprosto zanedbatelných sérových koncentrací (< 0,4 % podané dávky). Naproti tomu jsou zaznamenávány vysoké koncentrace léčiva ve stolici. Průměrná koncentrace léku po 3 dnech léčby rifaximinem v dávce 800 mg denně dosahovala 8 000 μg/g stolice a tato vysoká koncentrace přetrvávala 6 dní po ukončení léčebné kúry. In vitro studie potvrdily, že rozpustnost rifaximinu je až 120násobně větší ve žlučových kyselinách v porovnání s rozpustností ve vodě, což může teoreticky vysvětlovat vysoké koncentrace léčiva intraluminálně, především v proximální části tenkého střeva při běžném dávkování [1]. I když je rifaximin účinný proti velkému spektru střevních bakterií, vykazuje ve svém komplexním účinku na střevní mikrobiota také některé mimořádné účinky, kterými se odlišuje od všech ostatních antibiotik nebo chemoterapeutik. Stimuluje růst některých probioticky působících bakteriálních kmenů, jako jsou bifidobakterie, laktobacily nebo Fecalibacterium prausnitzi a zvyšuje bakteriální diverzitu. Navíc bylo prokázáno v pokusech na experimentálních zvířatech s indukovanou chemickou kolitidou, že má vlastní protizánětlivý efekt zprostředkovaný přes PXR (pregnane-X-receptor), který snižuje tvorbu některých prozánětlivých cytokinů zablokováním aktivace NF-kB [2]. Z hlediska mikrobiologického nevede ke vzniku rezistentních bakteriálních kmenů a nevede k dlouhodobé devastaci střevních mikrobiotů tak, jak je tomu často při léčbě jinými širokospektrálně působícími antibiotiky [3].
Hlavními indikacemi k zavedení terapie rifaximinem je v praxi gastroenterologů symptomatická, nekomplikovaná divertikulární choroba tlustého střeva a prevence recidivy divertikulitidy v podobě cyklické, dlouhodobé terapie, dále léčba gastrointestinálních infekcí, včetně průjmů cestovatelů, nasedající infekce u nemocných s idiopatickými střevními záněty, lehčí forma pouchitidy. Využívá se také v léčbě syndromu bakteriálního přerůstání na tenkém střevě (SIBO). V hepatologické praxi se rifaximin osvědčil jako preventivní léčba jaterní encefalopatie. Tento lék velmi dobře odpovídá základním kritériím stanovených Herbert Du Pontem a Charlesem Ericssonem na počátku 90. let minulého století, kteří se snažili určit základní kritéria pro optimální antibiotikum indikované v léčbě gastrointestinálních infekcí:
a) vysoká protibakteriální účinnost;
b) minimální možnost vstřebávání z trávicího ústrojí a co nejnižší systémový vliv;
c) minimální dopad na vznik bakteriální rezistence;
d) minimální vedlejší účinky tak, aby se antibiotikum mohlo využít u dětí, starších a polymorbidních pacientů a u těhotných žen.
Hlavní předností antibiotik využívaných v terapii infekčních a zánětlivých procesů v trávicí trubici je tedy velmi nízká rozpustnost, a tím také omezená možnost resorpce. Antibiotika, která splňují tyto požadavky na minimální rozpustnost a velmi omezenou vstřebatelnost, jsou nejen rifaximin, ale také amino-glykosidová antibiotika, vankomycin, teicoplanin, fidaxomycin a ramoplanin. Některá z těchto protibakteriálních antibiotik (vankomycin, fidaxomycin, rifaximin) jsou využívána v terapii infekce Clostridiodes difficile, která osídluje tlusté střevo po předcházející terapii širokospektrálními antibiotiky (clindamycin, amino-peniciliny) nebo se objevuje u imunokompromitovaných nemocných léčených imunosupresivní a/nebo biologickou léčbou, typicky je tomu u pacientů s ulcerózní kolitidou. Paramomycin se uplatňuje v léčbě parazitárních infekcí způsobených amébou, lamblií nebo kryptosporidiozou; neomycin a rifaximin jsou spíše využívány k terapii bakteriálních gastrointestinálních infekcí a v léčbě dysmikobie. Farmakokinetické studie potvrdily velmi nízkou, zanedbatelnou resorpci rifaximinu ze střeva, takže močová exkrece léčiva dosahuje v průměru 0,03 % podané denní dávky. Více než 99 % podané látky se tedy ze střeva nevstřebává.
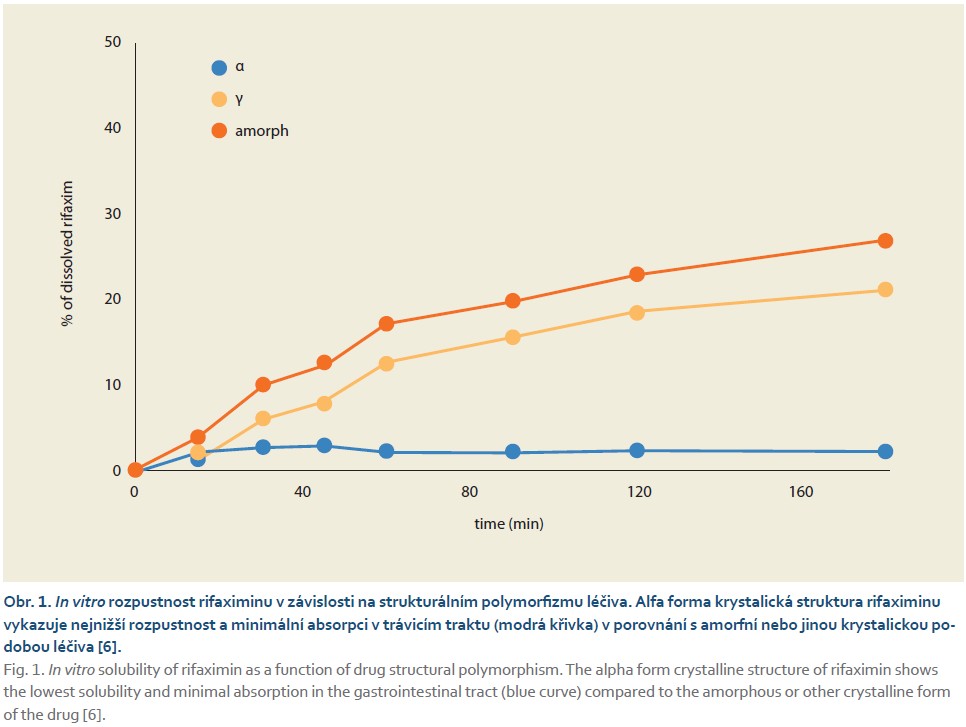
Strukturální polymorfizmus, který se objevuje u řady léčiv, je charakterizován tím, že molekuly příslušného léčiva se mohou shlukovat do různých krystalických nebo nekrystalických (amorfních) struktur. Různé krystalické podoby léčiva pak mohou mít vliv na jeho fyzikální a chemické vlastnosti léky, zahrnující stabilitu, rozpustnost, vstřebatelnost a systémovou dostupnost v organizmu. Polymorfické změny se u léčiva mohou objevit při jeho výrobě, ale také při skladování léku. V případě rifaximinu může transformace různých krystalických forem měnit jeho biologickou dostupnost, a tím také farmakodynamický efekt léčiva. Rifaximin se vyskytuje v krystalické a v amorfní podobě. Krystalická struktura rifaximinu má celkem pět variant (alfa, beta, gama, delta a epsilon), přičemž nerozpustná, resp. minimálně rozpustná je pouze a forma léčiva. Přítomnost většího podílu ostatních krystalických forem rifaximinu (beta, gama, delta a epsilon), nebo amorfní verze rifaximinu zvyšuje podíl léčiva, které je rozpuštěno a poté z trávicí trubice vstřebáno (obr. 1). Důkazy pro to poskytly studie na zvířatech, které potvrdily, že vstřebávání krystalické formy alfa a beta je zanedbatelné, kdežto resorpce krystalické formy epsilon je 6× vyšší a amorfní formy léčiva 400násobná oproti prvním dvěma variantám. Změna alfa formy na krystalickou beta formu rifaximinu může vést ke snížení koncentrace léčiva intraluminálně v trávicím ústrojí, a tudíž může mít nižší antibakteriální účinnost, změna alfa formy na gama krystalickou formu léčiva pak může významně zvýšit rozpustnost a také systémovou biologickou dostupnost léku [4]. V práci Toukabriho et al. [5] byly porovnávány fyzikálně-chemické vlastnosti čtyř preparátů obsahující rifaximin a tři generické preparáty s originálním lékem. Generická léčiva obsahovala větší podíl amorfní struktury rifaximinu a měla horší vlastnosti v porovnání s originálním preparátem obsahujícím pouze krystalickou alfa formu rifaximinu.
Z výše uvedeného je zřejmé, že malé strukturální změny ve složení léčiva mohou mít poměrně významné dopady na klinické využití rifaximinu v běžné praxi s ohledem na efektivitu a systémovou biologickou dostupnost. Jinými slovy pro optimální klinické využití rifaximinu bychom měli zohlednit složení, typ a formu vybraného léčiva.
Korespondenční autor
prof. MUDr. Milan Lukáš, CSc., AGAF
Klinické a výzkumné centrum pro střevní záněty
Klinické centrum ISCARE a. s. a 1. LF UK v Praze
Českomoravská 19
190 00 Praha 9
milan.lukas@email.cz
Literatura
1. DuPont HL. Review article: the antimicrobial effects of rifaximin on the gut microbiota. Aliment Pharmacol Ther 2016; 43(Suppl 1): 3–10. doi: 10.1111/ apt.13434.
2. Cheng J, Shah YM, Ma X et al. Therapeutic role of rifaximin in inflammatory bowel disease: clinical implication of human pregnane X receptor activation. J Pharmacol Exp Ther 2010; 335(1): 32–41. doi: 10.1124/ jpet.110.170225.
3. Lukáš M. Rifaximin v terapii idiopatických střevních zánětů. Gastroent Hepatol 2021; 75(1): 51–54. doi: 10.48095/ccgh202151.
4. Dharani S, Barakh SF, Afrooz F et al. Studying effect of glyceryl palmitostearate amount, manufacturing method and stability on polymorphic transformation and dissolution of rifaximin tablets. Int J Pharm 2020; 589: 119785. doi: 10.1016/j.ijpharm.2020.119785.
5. Toukabri I, Bahri S, Sfar S et al. Impact of crystal polymorphism of rifaximin on dissolution behaviour. Heliyon 2024; 10(5): e27131. doi: 10.1016/j.heliyon.2024.e27131.
6. Blandizzi C, Scarpignato C. Generic drugs in gastroenterology. Critical issues in bioequivalence and interference on therapeutic equivalence. Ther Perspect. 2014; 17: 1–43.